식약처, 중국 원료로 국내 제조 고혈압치료제 발암물질 발견…59개 품목 판매 중단
노은희 기자
입력일 2018-08-06 17:41
수정일 2018-08-06 17:41
발행일 2018-08-07
1면

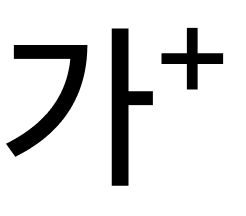

식품의약품안전처는 6일 국내 의약품 제조업체인 대봉엘에스가 중국산 원료를 사용해 제조한 고혈압치료제 원료의약품 ‘발사르탄’에서 암을 유발할 가능성이 있는 물질 ‘N-니트로소디메틸아민’(NDMA)이 검출돼 잠정 판매 및 제조 중지시켰다고 밝혔다.
식약처에 따르면 대봉엘에스는 중국 주하이 룬두사에서 원료의약품 이전 단계의 약리 활성 물질인 ‘조품’을 수입·정제해 발사르탄을 제조해왔다. 최근 3년간 국내 전체 발사르탄 원료의약품 시장에서 대봉엘에스가 제조한 발사르탄의 비중은 약 3.5%다. 이 중 일부 발사르탄에서 NDMA 잠정 관리 기준(0.3ppm)을 초과한 것으로 이번 조사를 통해 확인됐다.
문제가 된 대봉엘에스의 원료를 사용한 완제의약품은 22개사, 59개 제품이다. 해당 의약품을 복용 중인 환자 수는 이날 0시 기준 총 18만1286명으로 확인됐다. 59개 제품을 처방받은 환자는 진료받는 병원을 방문해 다른 의약품으로 재처방 및 재조제를 받을 수 있다. 처방은 기존 처방 중 남아있는 기간에 대해서만 가능하다. 의료기관을 방문하지 않고 약국에 가더라도 의약품 교환이 가능하며 재처방 및 재조제에 따른 환자 부담은 없다.
노은희 기자 selly215@viva100.com
랭킹뉴스