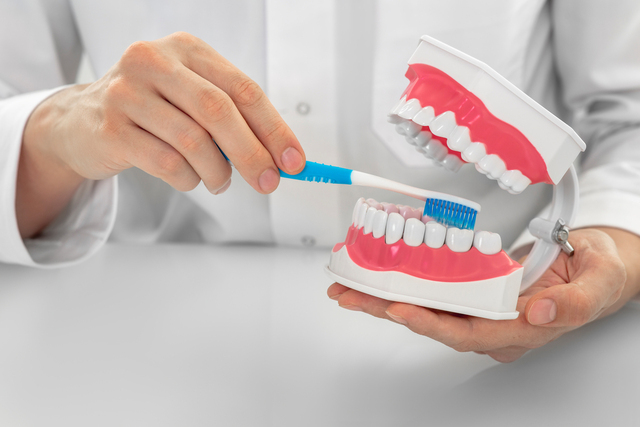
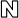동구바이오제약, 화성시 공장 증설에 33억5000만원 투자
2018-05-30 09:05 김선영 기자
노보 비만치료제 ‘삭센다’, 캐나다 리얼월드 연구서 일관된 효과
2018-05-30 09:05 김선영 기자
여름철 피부 기미 등에 맞춤형 색소침착 ‘토닝솔루션’ 주목
2018-05-29 17:30 김선영 기자
노바티스 혈소판감소증치료제 ‘레볼레이드’, 빈혈 적응증 추가
2018-05-29 09:06 김선영 기자
한독테바 ‘프레마네주맙’, 편두통 예방효과 연구 ‘JAMA’ 게재
2018-05-29 09:05 김선영 기자
머크, 美 ASCO서 항암제 파이프라인 소개 … 항PD-L1 면역항암제 ‘바벤시오’ 등
2018-05-29 09:02 김선영 기자
종근당, 에자이와 치매치료제 ‘아리셉트’ 등 2품목 공동판매
2018-05-29 09:02 김선영 기자
일동제약, 부패방지경영시스템 ‘ISO37001’ 인증
2018-05-29 09:01 김선영 기자
식약처, 구강용 ‘벤조카인’ 제제 24개월 미만 영아 사용금지
2018-05-29 09:01 김선영 기자
장봉근 제이비케이랩 대표, 안토시아닌 암피로증후군 개선 효과 발표
2018-05-29 09:01 김선영 기자
[병원 단신] 서울대치과병원, ‘가지런한 영구치’ 건강강좌 31일 … 송지수 소아치과 교수 강연
2018-05-29 09:00 김선영 기자
심평원, ‘보건의료 빅데이터 창업아이디어 공모전’…7월 11일까지
2018-05-27 15:52 김선영 기자
유럽 PRAC, 자궁근종치료제 ‘울리프리스탈’ 간기능검사 후 신규투여 가능
2018-05-26 09:58 김선영 기자
녹십자웰빙 간기능개선제 ‘라이넥’, 동물실험서 스트레스 감소효과
2018-05-26 09:56 김선영 기자
강동경희대한방병원, 암환자 대상 ‘십전대보탕’ 피로 개선효과 연구 참여자 모집
2018-05-26 09:55 김선영 기자
동화약품, 화장품 ‘활명’ 기초 스킨케어 5종 출시
2018-05-26 09:55 김선영 기자
동구바이오제약, 줄기세포 추출키트 ‘스마트엑스’ 국책과제 선정
2018-05-26 09:54 김선영 기자
獨 머크, 전세계 과학자 대상 연구 공모전 … 창립 350주년 기념
2018-05-26 09:54 김선영 기자
안국약품, 2018 신입·경력 상반기 공채 … 6월 3일까지 접수
2018-05-26 09:54 김선영 기자
차바이오텍, 이영욱·최종성 공동대표 체제로 변경
2018-05-26 09:53 김선영 기자
랭킹뉴스