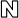네이처셀, 알츠하이머 치매 줄기세포 치료기술 日서 세계 최초 상용화

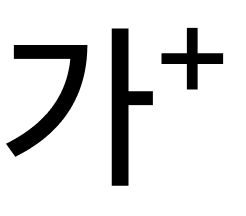

바이오스타 줄기세포기술연구원(원장 라정찬)은 일본 협력병원인 후쿠오카 트리니티 클리닉이 19일 열린 특정인정재생의료위원회 심사에서 알츠하이머 치매 치료에 관한 승인 적합 결정을 받았다고 20일 밝혔다. 심사 결과는 일본 후생노동성에 전달되며, 이 달 안에 정식 치료가 시작된다.
일본은 ‘재생의료 안전성 확보에 관한 법률’에 따라 배양한 자가성체줄기세포 치료를 의약품이 아니라 치료기술로 승인 받을 수 있다. 재생의료 분야 전문가로 구성된 특정인정재생의료위원회가 줄기세포 치료에 대한 안전성과 유효성을 검토한 후 승인 적합 결정을 내리게 되면, 그 결정을 일본 후생노동성에 제출하고 줄기세포 치료를 실시할 수 있도록 했다.
연구원에 따르면 규슈 특정인정재생의료위원회는 줄기세포전문가, 생명윤리전문가, 규슈의과대학 교수, 변호사, 의사, 일반 소비자 등 각 분야의 전문가 16명으로 구성되어 치료계획을 심사하였으며, 신청사와의 질의응답, 전문가들간의 충분한 토론 등을 거쳐 2시간 30분동안 진행되었다. 또한 환자에 대한 리스크와 혜택 등이 고려된 후 투표에 의해 결정이 이루어졌다. 이번 승인으로 후쿠오카 트리니티 클리닉은 세계 최초이자 유일하게 우리나라 연구진이 개발한 줄기세포로 알츠하이머 치매를 치료할 수 있게 됐으며, 이에 따라 한국은 물론 전 세계 알츠하이머 치매 환자들이 일본에서 치료를 받을 수 있게 됐다.
라정찬 박사는 “한국의 여건이 개선되고 있지 않으므로 당분간 모든 투자와 역량을 일본과 미국에 집중할 것”이라며 “한국, 중국, 미국 등 전세계 치매 환자는 물론이고, 이미 승인 받아 치료중인 퇴행성 관절염 환자들도 일본에서 성공적인 줄기세포 치료를 받을 수 있도록 힘쓰겠다”고 전했다.
한편, 알츠하이머 치매 치료를 위한 줄기세포 기술은 라정찬 박사가 2008년 자신의 몸에 직접 정맥 내 주사법을 시험해 가면서 바이오스타 줄기세포 기술연구원이 10년 이상에 걸쳐 개발했다. 정맥 내에 자가지방유래 줄기세포를 배양하여 투여하는 방식으로 2주 간격으로 회당 2억 셀씩, 총 10회에 걸쳐 투여한다. 연구원이 세계 최초로 개발한 정맥 투여 방식은 미국 임상시험에서 안전성을 확인했으며, 암 발생에 영향을 주지 않는다는 임상연구 결과도 발표된 바 있다.
노은희 기자 selly215@viva100.com